9 空調機の冷却熱量 ~湿り空気線図の用語~
空調機といっても、一般家庭にあるエアコンから大型の倉庫をまるごとの空調機まで幅が広いです。
でも大丈夫。基本は分散機と同じ、熱交換をするだけです。恐れることはありません。冷却熱量の計算が若干違うだけで、後の流れは分散機と同じです。
さっそく、冷却熱量について考えていきましょう。
冷やしたり温めたりする対象が空気になります。
空気は目に見えないので、直感的に理解するのが難しいかもしれません。湿度80%で25℃と湿度50%で30℃のどっちのエネルギーが大きい?といわれても直観的に答えるのは難しと思います。調べると、湿度80%で25℃の方が大きいです。
直感的に理解できなければ、調べれば済むことです。 というわけで、調べ方を学んでいきましょう。
空調機の冷却熱量を計算するのは、そんなに難しくはありません。難しいのは前提条件どうやって決めるかです。
難しい問題は次回以降でやるとして、今回は冷却熱量の計算方法だけをやります。 空調機の冷却熱量を計算するためには、湿り空気線図というグラフを使います。このグラフを完全に表現できる式はありません。現在最も有力なのは、「ウェクスラー・ハイランド(Wexler-Hyland)の式」と呼ばれるものですが、式を見たらわかるように、

複雑過ぎて、何が何やらわかりません。この式を解くぐらいなら、湿り空気線図を読み取る方が簡単で確実です。ただ、湿り空気線図の読み方がちょっと複雑です。
まずは、言葉の説明から始めます。
- 乾球温度 単位:℃
乾湿計は、二つの普通の温度計が並んでいて、左はそのまま(乾球)で、右は球をガーゼで包んで下端を水に浸してあります(湿球)。左の乾球で読み取った値が乾球温度です。
- 湿球温度 単位:℃
右の湿球で読み取った値が湿球温度です。
- 相対湿度 単位:%
普通に湿度といえば、相対湿度のことです。 相対湿度は容器の最大量に対して何%の水蒸気が入っているか、つまり空気中の水分の「割合」を示す尺度です。これを電車にたとえれば、相対湿度50%=座席が50%埋まっているということになります。ただし相対湿度だけでは乗客の混み具合がわかるだけで、実際の乗客の人数や乗車定員はわかりません。混み具合を知りたい場合はそれだけで十分です。
- 絶対湿度 単位:kg/kg(空気1kgに含まれる水分の量)
絶対湿度は、空気中の水分の「量」を示します。これを同じように電車でたとえると、絶対湿度50kg/kg=乗客数が50人であるということになり、「何人の乗客が乗っているか」がわかります。この場合、乗客数はわかりますが、電車が混んでいるのか空いているのかがわかりません。

- 水蒸気分圧 単位:kPa
水蒸気の分圧のことです。水蒸気は知っていると思うので分圧について説明します。
気軽に分圧という言葉が出てきます。気軽に使っている理由は、ニュートンの法則で重力という言葉が一般的なように、分圧の法則(ドルトンの法則)があるからです。
分圧の法則は、『定温定圧の条件で数種の理想気体を混合して1つの混合気体をつくるとき、混合気体の占める体積は混合前に各気体が占めていた体積の和に等しく、また混合気体の圧力(全圧)は各気体の分圧の和に等しい』というものです。高校で物理を真剣に勉強していいたらピン!とくるかもしれませんが、ちょっと表現が難しいですね。この表現を理解するためには、2つの法則を知っておく必要があります。
ボイルの法則、シャルルの法則がそれで、この2つの法則はボイル・シャルルの法則として1つにまとめられたりもします。

これは理解するというよりも、こういうもんなんだと納得するしかありません。体積が半分になったら圧力は倍になり、圧力が半分になったら体積は倍になるということを示しています。だから何?と思う人がいるかもしれませんが、この法則は日常生活に直結しています。特に圧縮エアーを取り扱っている人は重要なことです。コンプレッサーでは1MPaぐらいの圧縮エアーを作ることが多いと思います。圧縮エアーはエアータンクとかエアー配管とかの決められた体積で圧力だけが上がります。ボイル・シャルルの法則に従えば、圧力pが約10倍、体積Vは一定ということになります。じゃあ、温度Tは?恐ろしく高温になるのです。実際には放熱しているので、エアータンクは温かいぐらいの温度となります。逆に、エアーガンとかでエアーを体に当ててみると、冷たいと感じたことはありませんか?圧縮エアーの吹き出し口付近では急激に圧力が変化します。同時に体積も変化します。でも、圧力は常圧までしか下がらないのに、体積はほぼ無限大なので、結果として温度が下がることになるわけです。
そんなボイル・シャルルの法則で分圧の法則を適用してみます。分圧の法則は定温定圧を条件としているので、体積Vも一定ということになりますね。とある気体AとBを混ぜて混合気体を作る場合、圧力と温度を揃えておけば、それぞれの体積は一定になるので混合気体の体積はVA+VBになります。じゃあ、今度は体積と温度を一定にしてみたらどうでしょう。混合気体の圧力はPA+PBになります。ほら、圧力(分圧)の和になったでしょ。 このことを空気中の水蒸気について示したのが水蒸気分圧ということで、空気中に含まれる水蒸気の量ということになります。
- 顕熱比
何かを溶かしたり、蒸発させたり、凝縮させたりするとき顕熱や潜熱という言葉が頻繁に出てきます。まずはそこから。
氷が水へと状態(相が)変化するとき、変化している間は加熱されているにもかかわらず温度は一定値のままです。また、水が水蒸気へと状態変化するとき、変化している間は加熱されているにもかかわらず温度は一定値のままです。
逆に、水が氷へと状態(相が)変化するときも、変化している間は冷却されているにもかかわらず、温度は一定値のままです。同様に水蒸気が水へと状態(相が)変化するときも、変化している間は、冷却されているにもかかわらず温度は一定値のままです。
状態を変化させる(相を変化させる)ために熱が使われているからです。
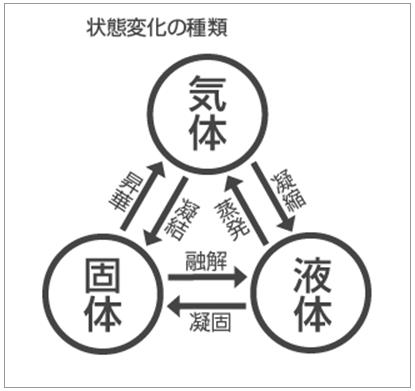
図のように、物質が固体から液体、液体から気体、固体から気体、あるいはその逆方向へと状態変化(相変化)する際に必要とする熱のことを「潜熱」と言い、温度変化を伴いません。
一方、温度変化を伴う熱を「顕熱」と言います。
顕熱比は、全熱(潜熱+顕熱)に対する顕熱の比です。つまり、与えたエネルギーに対して温度変化に寄与する比率を示しています。

- 比エンタルピー 単位:kJ/kg〔DA〕
単位質量当たりのエンタルピーのことなんですが、エンタルピーって?
エンタルピーは次式で定義される値です。
エンタルピー H は内部エネルギー U、圧力 p、体積 V を用いて
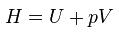
内部エネルギーというのは、その物体の運動エネルギーと位置エネルギーをあわせたものと考えてください。要は物体の持ち得るエネルギーです。
つまりエンタルピーは、
エンタルピー=(エネルギー)+(圧力)×(体積)
と表現できます。
ある気体の温度をT1℃からT2℃に上げたい。それにはふたつの手段があります。気体を圧縮する等の仕事をするか、ヒーター等で加熱するか、少なくともどちらかを行わなければなりません。
熱量と仕事の和が10になるように加えれば、T1℃からT2℃になるとします。つまり、「熱量が1なら仕事は9」や「熱量が10なら仕事が0」といった感じです。
T1℃からT2℃にするには、10の熱量と仕事の合計が必要です。逆に言えば、合計が10でさえあれば仕事も熱量も加える量は自由です。
温度という量は物質の状態を決めるひとつの量なので経路に依存しません。T1℃からT2℃に上げたなら、上げた方法(経路)はどうでもいいのです。
ここで、エンタルピーの式に戻ってみましょう。
右辺のpVはボイル・シャルルの法則からも温度に直結する値であることが解ると思います。内部エネルギーUもある物質の状態を表す状態量なので、エンタルピーは経路に依存しない状態量ということになります。このことを言い換えると、状態変化の経路を無視して、エネルギーの量から物質の状態を量ることができる量ということになります。
実際の使い方は逆で、状態Aから状態Bに空気を変化させたい場合、エンタルピーの変化量から、状態を変化させるために必要なエネルギー量を推測します。
- 熱水分比 単位:kJ/kg
熱水分比とは、空気に出入りする水蒸気によって、空気の持っている熱エネルギーがどれほど変化するかを示すものです。簡単に説明すると、エンタルピーの変化量と絶対湿度の変化の比のことをいいます。
- 比容積 単位:m3/kg〔DA〕
乾き空気1kgを含む湿り空気の容積。DAは乾き空気(Dry Air)1kgを表す
今回は用語の説明までにして、次回に実際に湿り空気線図の読み方を説明します。

